Dokumentationen fra forskellige systematiske gennemgange og meta-analyser af selen- og kræftundersøgelser viser en signifikant omvendt proportionalitet mellem selenindtag og/ eller plasma/serum-selenstatus og kræft [Lee; Hurst; Cai].
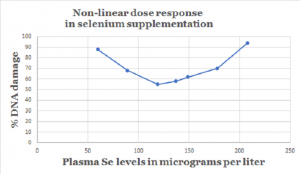
Der er nogle tegn på et U-formet forhold mellem plasma/serum-selenstatus og beskyttelse mod kræft [Hurst; Rayman]. Lav plasma/serum-selenstatus korrelerer klart med højere risiko for kræft. Høj plasma/serum-selenstatus korrelerer ikke med en øget kræftbeskyttende virkning. Nøglen er at finde de doseringsmængder og den efterfølgende plasma/serum status, der giver den bedste beskyttelse mellem de to yderpunkter.
Evaluering af bevismaterialet fra offentliggjorte studier er kompliceret. Vi skal huske, at følgende faktorer påvirker forholdet mellem selenstatus og/eller -indtagelse og kræftrisiko:
- Typen af selentilskud
- Kostens selenindhold ved undersøgelsesstart
- Plasma/serum-selenstatus ved undersøgelsesstart
- Undersøgelsesdeltagernes risikoniveau
- Typen af kræft
Typen af selentilskud og kræftrisiko
Baseret på bevismateriale fra randomiserede kontrollerede undersøgelser er den effektive form af selentilskud til forebyggelse af kræft, organisk selengær [Clark, Yu]. Effektive selengær-præparater som dem, der blev anvendt i PRECISE-undersøgelserne, indeholder organisk l-selenomethionin, Se-methylselenocystein (= forbindelsen findes i hvidløg) og tæt på 30 andre selenforbindelser [Larsen 2004].
Vær opmærksom på, at selengær-præparaterne indeholder en organisk form for l-selenomethionin, som er den form, der findes naturligt i paranødder, plantefrø og bælgplanter. L-selenomethionin i selengær-præparater er ikke det samme som det syntetiske l-selenomethionin, der blev anvendt i SELECT-studiet [Lippman, Klein].
Kosttilskud med selengær er forholdsvis meget mere sikre selen-kosttilskud [Schrauzer 2006].
Seleniveauer og kræftrisiko ved undersøgelsesstart
Alt taget i betragtning foretrækkes undersøgelser, der ser på sammenhængen mellem plasma- eller serumselen-koncentrationer ved undersøgelsesstart og kræftrisiko frem for undersøgelser, der ser på sammenhængen mellem selenindtagelsen ved undersøgelsesstart og kræftrisiko.
Der er to årsager:
1. Blod-seleniveauer kan måles mere præcist end måling af selenindtagelsen fra kosttilskud, fordi de fleste data fra indtagelse af kosttilskud kommer fra deltagernes selvrapportering:
- Data fra spørgeskemaer om måltidshyppighed
- Data fra spørgeskemaer med baggrundsoplysninger om brugen af kosttilskud
- Data fra spørgeskemaer med supplerende oplysninger
2. Selv når undersøgelsens deltagere rapporterer, at de spiser de samme fødevarer i de samme mængder, kan der være regionale variationer i landbrugsjordens selenindhold og i fødevarerne. 227 g (8 oz) ris fra én egn af landet kan godt indeholde mindre selen end 227 g ris fra en anden egn.
Selentilskud og forskellige kræftformer
Dr. Cai og kolleger konkluderede i en meta-analyse fra 2016 om seleneksponering og kræftrisiko, at højere seleneksponering er forbundet med nedsat risiko for følgende specifikke kræftformer:
- Brystkræft
- Spiserørskræft
- Mavekræft
- Lungekræft
- Prostatakræft
Imidlertid er højere seleneksponering endnu ikke utvetydigt forbundet med nedsat risiko for blærekræft, tyktarms- og endetarmskræft eller hudkræft [Cai].
Dosisrespons på selen og kræftrisiko
En tommelfingerregel der tidligere har været meget udbredt siger, at det medfører et fald i risikoen for kræft på ca.10% for hver gang plasma/serumkoncentrationen af selen øges med 10 mikrogram per liter. [Hurst].
Denne tommelfingerregel bør understøttes af mere empiriske beviser, og husk: Den kan kun gælde inden for grænserne af den U-formede kurve. De lave og øvre grænser for effektiviteten af selentilskud mod udvikling af kræft skal også fastlægges mere præcist.
Optimal plasma/serum-seleniveau og kræftrisiko
Data fra undersøgelsen af ernæringsmæssig forebyggelse af kræft (NPC-studiet), som blev udført i USA af professor Larry Clark og hans kolleger, viste, at den beskyttende virkning af selen mod udviklingen af nogle kræftformer begyndte at kunne ses ved en nedre grænse på 120 mikrogram selen pr. liter plasma [Clark].
Dr. Hurst og kolleger i Storbritannien gennemførte en meta-analyse af studier af selenstatus og risikoen for prostatakræft. Data fra deres meta-analyse viste, at der var en gradvis nedsat risiko for den samlede andel af prostatakræft og for fremskreden prostatakræft i området fra 60 mikrogram selen pr. liter plasma op til 170 mikrogram pr. liter.
Ved niveauer over 170 mikrogram pr. liter blev den beskyttende virkning af selentilskud udfladet, og yderligere selen ophørte med at virke beskyttende. Med andre ord giver selentilskud ikke den samme beskyttelse hos personer der er fyldt med selen, som det gør hos personer der mangler selen [Hurst].
Forskelle mellem NPC-studiets resultater og SELECT-studiets resultater
Der var to store forskelle i udformningen af NPC-studiet af kræft [Clark] og i udformningen af SELECT-studiet [Lippman; Klein]:
- Tilskudets art: Organisk selengær i NPC-undersøgelsen versus syntetisk l-selenomethionin i SELECT-studiet
- Den gennemsnitlige serumselen-status hos deltagere var ved forsøgets start: 113 mikrogram pr. liter i NPC-undersøgelsen og 135 mikrogram pr. liter i SELECT-undersøgelsen [Lippman]
Disse to forskelle – Typen af selentilskud og serum-selenstatus ved undersøgelsesstart – kan forklare, hvorfor NPC-undersøgelsen viste signifikante reduktioner i risikoen for kræft og SELECT undersøgelsen ikke gjorde.
Andre faktorer der vedrører selentilskud og kræftrisiko
I en kommende artikel kunne jeg tænke mig at adressere andre faktorer, som kan påvirke den beskyttende effekt af selentilskud mod kræft:
- Alder
- Køn
- Forskellige selenoproteiners optimale aktivitetsniveau
- Race
- Ryger/ikke-ryger
På nuværende tidspunkt peger de videnskabelige data, der er opsummeret ovenfor, på den bedste effekt fra selengær-præparater til kræftforebyggelse.
Kilder
Cai, X., Wang, C., Yu, W., Fan, W., Wang, S., Shen, N., & … Wang, F. (2016). Selenium Exposure and Cancer Risk: An Updated Meta-analysis and Meta-regression. Scientific Reports, 619213. doi:10.1038/srep19213
Chiang, E. C., Shuren, S., Kengeri, S. S., Xu, H., Combs, Jr., G. F., Morris, J. S., Bostwick, D. G., & Waters, D. J. (2010). Defining the Optimal Selenium Dose for Prostate Cancer Risk Reduction: Insights from the U-Shaped Relationship between Selenium Status, DNA Damage, and Apoptosis. Dose Response, 8(3): 285–300. doi: 10.2203/dose-response.09-036.
Clark, L. C., Combs, G. J., Turnbull, B. W., Slate, E. H., Chalker, D. K., Chow, J., & Taylor, J. R. (1996). Effects of selenium supplementation for cancer prevention in patients with carcinoma of the skin. A randomized controlled trial. Nutritional Prevention of Cancer Study Group. JAMA, 276(24), 1957-1963.
Hurst, R., Hooper, L., Norat, T., Lau, R., Aune, D., Greenwood, D. C., & Fairweather-Tait, S. J. (2012). Selenium and prostate cancer: systematic review and meta-analysis. The American Journal of Clinical Nutrition, 96(1), 111-122. doi:10.3945/ajcn.111.033373
Klein, Eric A, Ian M, Jr Thompson, Catherine M Tangen, John J Crowley, M Scott Lucia, Phyllis J Goodman, and Laurence H Baker, et al. 2011. “Vitamin E and the risk of prostate cancer: the Selenium and Vitamin E Cancer Prevention Trial (SELECT).” JAMA 306, no. 14: 1549-1556. MEDLINE with Full Text, EBSCOhost (accessed December 5, 2017).
Larsen, E. H., Hansen, M., Paulin, H., Moesgaard, S., Reid, M., & Rayman, M. (2004). Speciation and bioavailability of selenium in yeast-based intervention agents used in cancer chemoprevention studies. Journal of AOAC International, 87(1), 225-232.
Lee, E., Myung, S., Jeon, Y., Kim, Y., Chang, Y. J., Ju, W., & … Huh, B. Y. (2011). Effects of selenium supplements on cancer prevention: meta-analysis of randomized controlled trials. Nutrition and Cancer, 63(8), 1185-1195. doi:10.1080/01635581.2011.607544
Lippman, S. M., Klein, E. A., Goodman, P. J., Lucia, M. S., Thompson, I. M., Ford, L. G., & Coltman, C. J. (2009). Effect of selenium and vitamin E on risk of prostate cancer and other cancers: the Selenium and Vitamin E Cancer Prevention Trial (SELECT). JAMA, 301(1), 39-51. doi:10.1001/jama.2008.864
Rayman, M. P. (2012). Selenium and human health. Lancet (London, England), 379(9822), 1256-1268. doi:10.1016/S0140-6736(11)61452-9.
Schrauzer, G. N. (2006). Selenium yeast: Composition, quality, analysis, and safety. Pure Appl. Chem., 78(1), 105–109. doi:10.1351/pac200678010105
Yu, S. Y., Zhu, Y. J., & Li, W. G. (1997). Protective role of selenium against hepatitis B virus and primary liver cancer in Qidong. Biological Trace Element Research, 56(1), 117-124.
Oplysningerne i denne artikel er ikke ment som lægehjælp og bør ikke bruges som sådan.
